විශේෂාංග
ජලීය ද්රාවණයක ක්ලෝරීන් අයන සාන්ද්රණය හෝ මායිම් නිර්ණය සහ දර්ශක ඉලෙක්ට්රෝඩ ෆ්ලෝරීන්/ක්ලෝරීන් අයන මගින් අයන සාන්ද්රණයේ ස්ථායී සංකීර්ණ සෑදීම සඳහා මාර්ගගත අයන ඉලෙක්ට්රෝඩය මනිනු ලැබේ.
| මිනුම් මූලධර්මය | අයන වරණීය විභවමිතිය |
| මිනුම් පරාසය | 0.0 ~ 2300mg/L |
| ස්වයංක්රීය උෂ්ණත්වයවන්දි පරාසය | 0~ ~99.9℃,25℃ උෂ්ණත්වයක් සහිතවයොමු උෂ්ණත්වය |
| උෂ්ණත්ව පරාසය | 0~ ~99.9℃ උෂ්ණත්වය |
| ස්වයංක්රීය උෂ්ණත්වයවන්දි | 2.252K,10,000,පීටී 100,PT1000 ආදිය |
| පරීක්ෂා කරන ලද ජල සාම්පලය | 0~ ~99.9℃,0.6MPa |
| මැදිහත්වීම් අයන | AL3+,Fe3+,OH-ආදිය |
| pH අගය පරාසය | 5.00~ ~10.00PH |
| හිස් විභවය | > 200mV (ඩයෝනීකරණය කළ ජලය) |
| ඉලෙක්ට්රෝඩ දිග | 195 මි.මී |
| මූලික ද්රව්ය | පීපීඑස් |
| ඉලෙක්ට්රෝඩ නූල් | 3/4 පයිප්ප නූල්()එන්පීටී) |
| කේබල් දිග | මීටර් 5 යි |
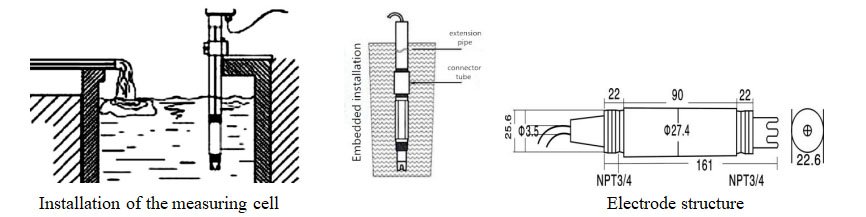
අයනයක් යනු ආරෝපිත පරමාණුවක් හෝ අණුවකි. එය ආරෝපණය වන්නේ පරමාණුවේ හෝ අණුවේ ඇති ප්රෝටෝන ගණනට ඉලෙක්ට්රෝන ගණන සමාන නොවන බැවිනි. පරමාණුවක ඇති ඉලෙක්ට්රෝන ගණන පරමාණුවේ ඇති ප්රෝටෝන ගණනට වඩා වැඩිද අඩුද යන්න මත පදනම්ව පරමාණුවකට ධන ආරෝපණයක් හෝ සෘණ ආරෝපණයක් ලබා ගත හැකිය.
පරමාණුවක් තවත් පරමාණුවකට ආකර්ෂණය වන විට, එහි ඉලෙක්ට්රෝන සහ ප්රෝටෝන අසමාන සංඛ්යාවක් ඇති බැවින්, එම පරමාණුව ION ලෙස හැඳින්වේ. පරමාණුවේ ප්රෝටෝන වලට වඩා ඉලෙක්ට්රෝන වැඩි නම්, එය සෘණ අයනයක් හෝ ANION වේ. එහි ඉලෙක්ට්රෝන වලට වඩා ප්රෝටෝන වැඩි නම්, එය ධන අයනයක් වේ.
ඔබගේ පණිවිඩය මෙහි ලියා අපට එවන්න.















